Scoperto dal team di Andrea Ballabio al Tigem può cambiare il futuro di malattie come Parkinson, Alzheimer e altre malattie genetiche rare.

Ogni cellula del nostro corpo è una macchina incredibilmente sofisticata e complessa. È difficile mettere le mani tra i suoi ingranaggi e correggere eventuali difetti di funzionamento che nuocciono alla nostra salute.
Ecco perché una quindicina di anni fa la comunità scientifica ha salutato con grande entusiasmo la scoperta di un singolo gene che controlla l’intero processo con cui la cellula elimina i suoi prodotti di scarto, ne ricicla le parti utili e ne ricava energia. Attivando e disattivando quel singolo gene, chiamato TFEB, si accende e si spegne tutto questo macchinario, che ha un ruolo fondamentale nel funzionamento della cellula e, quando è difettoso, dà origine a una grande varietà di malattie.
Termovalorizzatore
Il processo di smaltimento e riciclo degli scarti cellulari, illustrato nella grafica qui sotto, prende il nome di autofagia ed è stato descritto nella seconda metà del ventesimo secolo. Il suo protagonista è il lisosoma, un organello, cioè un piccolo organo della cellula, che accoglie al suo interno le sostanze di scarto e le sminuzza usando delle forbici chimiche.
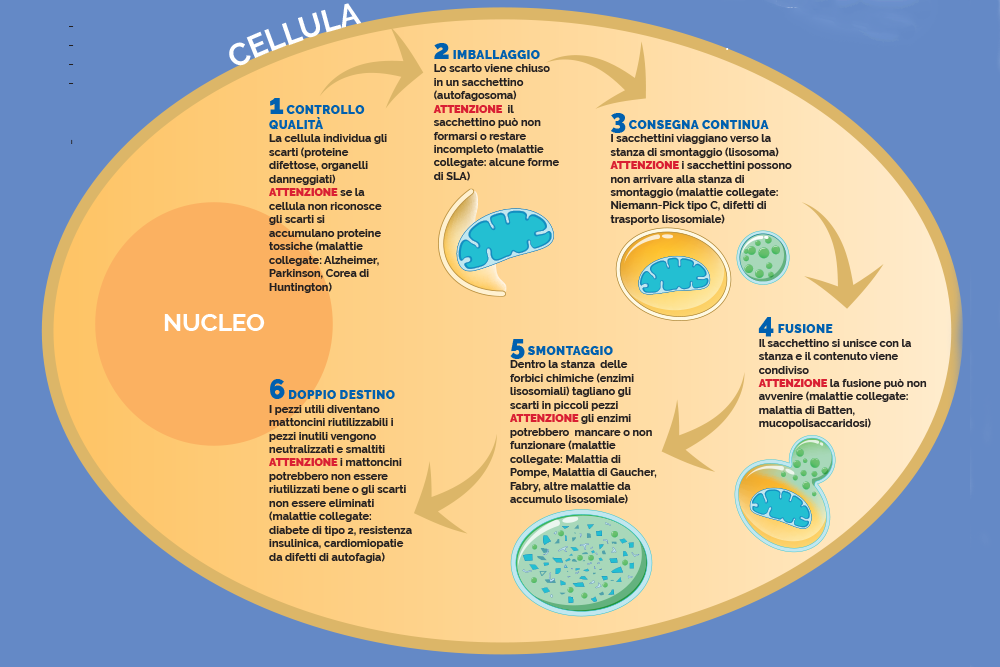
«Distrugge la spazzatura, ricicla le componenti utili e, nel farlo, produce energia proprio come un termovalorizzatore che usa i rifiuti come combustibile», spiega Andrea Ballabio, fondatore dell’Istituto Telethon di Genetica e Medicina (Tigem) di Napoli e suo direttore fino al 2024. «I lisosomi non funzionano a ritmo costante. Il loro numero e l’intensità del loro lavoro cambia nel tempo a seconda delle esigenze della cellula. Per esempio, subito dopo un pasto l’attività dei lisosomi è minima. Col passare del tempo e il protrarsi del digiuno, le cellule hanno bisogno di energia e ricorrono all’autofagia per ricavarla dalla distruzione degli scarti. Autofagia infatti vuol dire “mangiare se stessi”».
Meccanismo complesso
Ma in che modo la cellula accelera o rallenta il processo? Ballabio e i suoi collaboratori lo hanno scoperto studiando le cosiddette malattie da accumulo lisosomiale, una cinquantina di patologie genetiche rare caratterizzate dal malfunzionamento dei lisosomi e dall’accumulo nelle cellule dei rifiuti tossici che non vengono smaltiti correttamente.
«Ad essere danneggiati sono soprattutto i neuroni e i bambini che ne sono affetti vanno incontro a una rapida degenerazione del sistema nervoso», spiega il ricercatore. «Abbiamo esaminato i geni coinvolti nel meccanismo dell’autofagia e nel 2009 ne abbiamo identificato uno che li controlla tutti: TFEB. Quando si attiva, il numero dei lisosomi e l’intensità del loro lavoro aumentano. Quando si spegne, il macchinario rallenta».
A più di quindici anni da questo importante risultato, oggi TFEB è universalmente riconosciuto come l’interruttore generale dell’autofagia e oggetto di studio per il suo coinvolgimento in un gran numero di malattie.
«Oltre a quelle da accumulo lisosomiale, che sono rare, ce ne sono di più comuni legate a difetti dello stesso meccanismo: il Parkinson e l’Alzheimer, patologie neurodegenerative dell’adulto caratterizzate da malfunzionamento dei lisosomi e dall’accumulo di sostanze tossiche nei neuroni, un accumulo lento ma dagli effetti devastanti».
Risvolto terapeutico
I ricercatori del Tigem e altri gruppi nel mondo che lavorano in questo ambito hanno pensato allora di utilizzare TFEB a scopo terapeutico.
«Abbiamo riprodotto queste malattie su animali da laboratorio e poi abbiamo somministrato loro il gene TFEB, servendoci come mezzi di trasporto di virus resi innocui», spiega Ballabio. «L’effetto è stato rapido ed eclatante: i lisosomi attivati dal gene hanno ripulito le cellule dall’accumulo di scarti tossici, tanto che sulle pagine dei giornali TFEB si è guadagnato il nome di spazzino.
Questi esperimenti sono stati condotti a scopo dimostrativo, per verificare il coinvolgimento del gene nel meccanismo responsabile delle patologie e la possibilità di utilizzarlo per la loro cura, ma non è così che possiamo trattare le malattie da accumulo lisosomiale o il Parkinson. La terapia genica determina l’accensione permanente dell’interruttore TFEB, mentre noi cerchiamo un sistema per accenderlo e spegnerlo in base alle esigenze della cellula. Se un TFEB poco attivo provoca un dannoso accumulo di sostanze tossiche, un gene continuamente attivo crea altri problemi: determina una eccessiva proliferazione delle cellule e quindi lo sviluppo di tumori».
Giusto equilibrio
Un eccesso di attività dei lisosomi, per esempio, è all’origine di due malattie genetiche rare, la sindrome di Birt-Hogg-Dubé e la sclerosi tuberosa, caratterizzate dallo sviluppo di cisti e tumori alla pelle, ai reni e altri organi.
«Oggi quindi la ricerca in questo settore mira a mettere a punto un trattamento per accendere o spegnere a seconda delle necessità l’interruttore generale TFEB», spiega Ballabio. «Rispetto alla terapia genica, che è mirata in modo specifico a una singola malattia, un approccio di questo tipo sarebbe utilizzabile per il trattamento di diverse patologie, alcune rare, altre comuni».
Applicazioni future
Nel mondo c’è grande interesse su questo approccio, sia da parte di gruppi di ricerca pubblici, sia da parte di aziende farmaceutiche, che stanno investendo cifre notevoli sullo studio di TFEB.
«Per il momento, i potenziali trattamenti sono in fase di sperimentazione su colture cellulari o su animali. Nessuno è ancora arrivato ai test clinici, cioè su pazienti umani», osserva Ballabio. «Al Tigem stiamo lavorando in particolare sulla potenziale applicazione di questi strumenti terapeutici sulle malattie da accumulo lisosomiale, sul Parkinson, sulla sindrome di Birt-Hogg-Dubé e la sclerosi tuberosa».